von Dr. med. Jan Brandt, Prof. Dr. med. Jochen Sieper und Prof. Dr. med. Jürgen Braun, Klinikum Benjamin Franklin der Freien Universität Berlin
Die etablierten Behandlungsmöglichkeiten der entzündlichen
Wirbelsäulenerkrankungen (Spondyloarthritiden) sind unbefriedigend.
Die Langzeit-Antirheumatika ("Basismedikamente") Sulfasalazin, Methotrexat
und Cyclosporin haben eine gewisse Wirksamkeit bei Psoriasis-Arthritis.
Bei der Spondylitis ankylosans (Morbus Bechterew) wirkt Sulfasalazin
vor allem auf periphere (außerhalb der Wirbelsäule liegende)
Gelenke. Die Wirbelsäulenbeschwerden werden in fortgeschrittenen Stadien
nicht beeinflusst. Ob ein Einfluss in frühen Stadien vorhanden ist,
ist ungeklärt.
Der Krankheitsverlauf der Spondylitis ankylosans
kann durch Physiotherapie und nichtsteroidale Antirheumatika (NSAR) nur
beeinflusst, aber nicht aufgehalten werden. Bis zu 20% der Morbus-Bechterew-Patienten
sprechen schlecht oder gar nicht auf NSAR an. Auch die neuen, nur das Enzym
COX-2 hemmenden NSAR wie Rofecoxib stellen keine Lösung dieses
Problems dar (siehe Anhang).
Die Injektion eines Corticosteroids ins Gelenk wirkt zwar in diesem
Gelenk, kaum aber an allen übrigen Entzündungsstellen. Insgesamt
besteht ein dringender Bedarf an verträglicheren und besser wirksamen
Therapien.
Vor diesem Hintergrund hat die Pharmaindustrie eine neue Gruppe von
Medikamenten entwickelt, die sich die Erkenntnisse der Molekularbiologie
zunutze macht und bei den Autoimmunkrankheiten direkt ins Immungeschehen
eingreift. Man nennt diese Medikamente "Biologicals". Bei uns hat sich
für diese teuren High-Tech-Medikamente die Bezeichnung "Experimentelle
Therapie" eingebürgert.
Der Tumor-Nekrose-Faktor alpha (abgekürzt TNF-alpha)
ist ein Zytokin (Botenstoff, der Informationen zwischen Zellen transportiert),
das insbesondere von Makrophagen (Fresszellen), aber auch von T-Zellen
(ebenfalls weißen Blutkörperchen) produziert wird und dem eine
zentrale Rolle bei Entzündungsprozessen zugeschrieben wird.
In den letzten Jahren gab es zunehmend Hinweise darauf, dass TNF-alpha bei der chronischen Polyarthritis
eine zentrale Rolle in der Krankheitsentstehung spielt. Daraus entstand
die inzwischen eindrucksvoll bestätigte Hypothese,
dass eine Blockade von TNF-alpha eine neue Behandlungsmöglichkeit
für die chronischen Polyarthritis darstellen könnte.
Der erste für die Therapie der chronischen Polyarthritis
(rheumatoide Arthritis) zur Verfügung stehende TNF-alpha-Blocker war ein monoklonaler
Antikörper, der 1999 als Infliximab (Handelsname Remicade)
in den Handel kam. In der ersten Placebo-kontrollierten Studie aus dem
Jahr 1994 erhielten 73 Patienten mit aktiver rheumatoider Arthritis
eine Dosis von 1 oder 10 mg Infliximab pro kg Körpergewicht. Nach
einmaliger Infusion zeigten 44% der Patienten (bei 10 mg/kg sogar 79%)
eine wesentliche Besserung, während es in der Placebogruppe
(Behandlung mit einem Scheinpräparat zum Vergleich) nur 8% waren.
Mittlerweile wurde die Wirksamkeit der Anti-TNF-alpha-Therapie
bei Polyarthritis in verschiedenen Studien nachgewiesen. Zuletzt
konnte in einer großen placebo-kontrollierten Studie über ein
halbes Jahr mit 428 Patienten gezeigt werden, dass wiederholte Infusionen
mit Infliximab während einer Basistherapie mit Methotrexat
wirksamer sind als Methotrexat allein.
Ein weiteres Anti-TNF-alpha-Mittel
ist der TNF-alpha-Rezeptor Etanercept (Handelsname
Enbrel), der in Deutschland seit Anfang 2000 für die Behandlung der
chronischen Polyarthritis zugelassen ist. Er heftet sich ebenfalls
an die TNF-alpha-Moleküle und macht sie so unwirksam. Bei Polyarthritis-Patienten,
bei denen Methotrexat allein unzureichend wirkte, ist eine Kombination
aus Methotrexat und Etanercept ebenfalls wirksam.
Bei der Spondylitis ankylosans gibt es Hinweise,
dass TNF-alpha ebenfalls eine wichtige Rolle bei der Krankheitsentstehung
spielt. An Gewebeproben konnten wir kürzlich zeigen, dass im Iliosakralgelenk
von Morbus-Bechterew-Patienten TNF-alpha-Eiweiß vorhanden
ist, aber kein Bakterien-Eiweiß.
Ein weiterer Hinweis ist die Tatsache,
dass die Wirksamkeit von Anti-TNF-alpha in den letzten Jahren auch bei
Morbus Crohn nachgewiesen wurde. Der Morbus Crohn tritt mit der
Erkrankungsgruppe der Spondyloarthritiden häufig gemeinsam auf: 2060%
der Spondyloarthritis-Patienten haben Darmschädigungen wie beim Morbus Crohn.
In einer ersten Pilotstudie haben wir deshalb 11 Patienten
mit aktiver Spondylitis ankylosans mit je 3 Infusionen Infliximab
(5 mg pro kg Körpergewicht) behandelt. Das Alter der Patienten reichte
von 27 bis 56 Jahren (Durchschnitt 36 Jahre). Die durchschnittliche Erkrankungsdauer
betrug 5 Jahre (0,513 Jahre). Alle Patienten hatten eine hoch aktive Erkrankung.
Der Krankheitsaktivitätsindex (Bath Ankylosing Spondylitis Disease
Activity Index, BASDAI), dessen Skala von 0 bis 10 reicht, lag bei ihnen
zwischen 5,5 und 8,5 (Durchschnittswert 6,5). 10 der Patienten hatten vor
der Therapie erhöhte Werte des Entzündungs-Laborwerts CRP (C-reaktives
Protein). Fünf Patienten hatten Röntgen-Veränderungen
an der Wirbelsäule mit 3 oder mehr Syndesmophyten oder überbrückten
Wirbelkörpern.
Eine Patientin entwickelte 2 Wochen nach der ersten Infusion
einen Hautausschlag und wurde von der weiteren Behandlung ausgeschlossen.
Die übrigen 10 Patienten zeigten sofort nach der ersten Infusion eine
dramatische Besserung, die bei allen 10 Patienten über 6 Wochen anhielt.
In der 12. Woche (6 Wochen nach der 3. Infusion) hielt die Wirkung noch
bei 9 der 10 Patienten an. Der mittlere Krankheitsaktivitätsindex
BASDAI fiel in den ersten 4 Wochen von 6,5 auf 2 und blieb auf diesem niedrigen
Niveau (Bild 1). Der Mittelwert des CRP war 4 Wochen nach der ersten
Infusion von 15,5 auf 6,0 mg/l zurückgegangen (Bild 2). Auch
andere Messwerte für den Krankheitsverlauf (Beweglichkeit, Stärke
der Schmerzen) verbesserten sich bei 9 von 10 Patienten um mehr als 50
%. Zwei Patienten hatten eine chronische Gelenkentzündung im Knie
und im Sprunggelenk, die innerhalb der ersten zwei Tage nach der 1. Infusion
abklangen. Der durchschnittlich NSAR-Verbrauch sank um mehr als 50% des
Ausgangsverbrauchs. Fünf Patienten konnten die Einnahme ganz beenden.
Während der Studiendauer von 12 Wochen traten bei
5 von 11 Patienten harmlose Infektionen auf. Es handelte sich um 2 Mandelentzündungen,
eine Nasennebenhöhlenentzündung und eine Mittelohrentzündung,
die nach antibiotischer Therapie ausheilten. Ein Patient entwickelte eine
Herpes-Infektion an den Lippen.
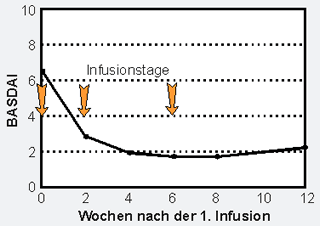 |
Bild 1: Mittelwert (Medianwert) der Krankheitsaktivität (Bath Ankylosing Spondylitis Disease Activity Index) vor, während und nach der dreimaligen Infusion des TNF-alpha-Blockers Infliximab |
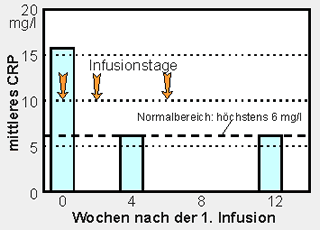 |
Bild 2: Mittelwert (Median) des Entzündungs-Laborwerts C-reaktives Protein vor, während und nach der dreimaligen Infusion des TNF-alpha-Blockers Infliximab |
Insgesamt zeigt diese Pilotstudie, dass eine TNF-alpha-Blockade mit Infliximab sehr wahrscheinlich auch bei einer aktiven Spondylitis ankylosans ein gut wirksames Behandlungskonzept darstellt. Fast alle Patienten hatten eine mehr als 50%ige Besserung der Krankheitsaktivität. Zukünftig muss in placebo-kontrollierten Studien sowohl die Kurzzeit- als auch Langzeit-Wirkung noch genauer untersucht werden. Nach den vorliegenden Ergebnissen scheint bei einer langfristigen Therapie im allgemeinen eine Infusion alle 6 Wochen nach einer anfänglichen Infusion in den Wochen 0, 2 und 6 sinnvoll zu sein. Individuelle Unterschiede sind möglich.
Die Ergebnisse lassen hoffen, dass mit der Blockade von TNF-alpha ein neues Therapiekonzept für die Spondylitis ankylosans zur Verfügung steht, das bei langfristigem Einsatz erstmalig in der Lage wäre, eine dauerhafte Besserung zu bewirken und möglicherweise auch die Versteifung aufzuhalten.
Eine andere Forschergruppe behandelte in einer offenen (nicht placebo-kontrollierten) Studie 6 Patienten mit schwerer Psoriasis-Arthritis, die schon vorher mit Methotrexat behandelt wurden, zusätzlich mit Infliximab. Die Patienten erhielten wie bei unserer Studie 3 Infusionen mit jeweils 5 mg Infliximab pro kg Körpergewicht und wurden insgesamt 10 Wochen lang beobachtet. Bei allen 6 Patienten trat eine schnelle und anhaltende Besserung der Gelenk- und Hautbeschwerden ein. Somit scheint eine Blockade von TNF-alpha auch bei Patienten mit schwerer Psoriasis-Arthritis, bei denen eine Methotrexat-Behandlung allein nicht ausreicht, eine vielversprechende neue Behandlungsmöglichkeit zu sein.
Folgende Nebenwirkungen kommen bei einer TNF-alpha-Blockade in Frage:
In der größten Placebo-kontrollierten Studie mit 428 Polyarthritis-Patienten, die ein halbes Jahr lang alle 4 bzw. 8 Wochen mit Infliximab behandelt wurden, wurden folgende Häufigkeiten von Nebenwirkungen beobachtet:
Infusions-bedingte Nebenwirkungen waren meistens mild
und besserten sich von selbst. Am häufigsten waren dies Kopfschmerzen
oder Schwindel. Nur 2 der 340 Patienten in der Infliximab-Gruppe
mussten wegen eines allergischen Nesselausschlags oder Atembeschwerden
die Teilnahme abbrechen.
Infektionen der Atemwege waren mit 2033% in der Infliximab-Gruppe
und 16% in der Placebogruppe (statistisch nicht signifikant) die häufigste
Nebenwirkung. Als gefährliche eingeordnete Infektionen traten in den
Infliximab-Gruppe und der Placebo-Gruppe mit jeweils 6% gleich häufig auf.
Unter einer Infliximab-Therapie kann es zur Bildung
von Doppelstrang-Antikörpern kommen, die beim Systemischen Lupus
erythematodes, (einer anderen entzündlich-rheumatischen Erkrankung)
eine Rolle spielen. In der oben zitierten Studie traten bei 16% der Patienten
Doppelstrang-Antikörper neu auf. Jedoch nur bei einem Patienten führte
dies zu einem medikamenten-verursachten Lupus erythematodes mit
typischen Hautveränderungen. Nach Beendigung der Therapie klangen
die Hautveränderungen ab.
Weil der Anti-TNF-alpha-Antikörper
auch als Antigen wirkt, kann es zur Bildung von Antikörpern gegen
diese Antikörper kommen. Nach einmaliger Infusion wurde dies bei 525%
der Patienten beobachtet. Eine gleichzeitige Therapie mit Methotrexat scheint
die Häufigkeit dieser Antikörper-Bildung zu verringern. Ob sich
die Anti-Antikörper-Bildung auf die Wirksamkeit der Therapie und auf
die Häufigkeit von Nebenwirkungen auswirkt, ist noch ungeklärt.
Malignome (bösartige Geschwulste) traten
unter den 340 Patienten der Infliximab-Gruppe bei 3 Patienten auf: ein
Brustkrebs-Rückfall, ein Hautkrebs und ein Lymphgewebe-Krebs. Die
beobachtete Häufigkeit war nicht höher, als es aufgrund einer
Datenbank der amerikanischen Gesundheitsbehörde bei der vorhandenen
Alters- und Geschlechtsverteilung zu erwarten war.
Insgesamt scheint nach den bisherigen Erfahrungen bei
der Polyarthritis und beim Morbus Crohn die Therapie mit Infliximab
eine gut verträgliche Behandlung zu sein. Insbesondere die Frage des
Krebsrisikos ist aber bis heute wegen der zu kurzen Anwendungszeit nicht
ausreichend sicher zu beantworten.
Ob die Anti-TNF-alpha-Behandlung
bei den Spondyloarthritiden auf die Dauer ähnlich unproblematisch
einzusetzen ist, müssen die noch ausstehenden Langzeitstudien zeigen.
Sollten weitere Untersuchungen die hier dargestellten
optimistisch stimmenden Ergebnisse zur Wirksamkeit und Verträglichkeit
bestätigen, bestünde zukünftig für Patienten mit einem
schweren Verlauf der Spondylitis ankylosans oder einer anderen Spondyloarthritis
eine hochwirksame neue Therapiemöglichkeit.
Wegen der nicht unerheblichen Kosten dieser Therapie
(3.300 bis 5.500 DM pro Infusion) wäre eine breite Diskussion in der
Rheumatologie über den Umgang mit dieser neuen Generation der "Biologicals"
und die Erarbeitung von Rahmenrichtlinien für ihren Einsatz wünschenswert.
Thalidomid (früher unter dem Handelsnamen Contergan
als Beruhigungsmittel verwendet) blockiert die entzündungsfördernde
Wirkung von TNF-alpha
auf indirektem Weg. Französische Forscher haben 1999 zwei Spondylitis-ankylosans-Patienten,
bei denen andere Medikamente nicht halfen, mit Thalidomid behandelt. Der
Beobachtungszeitraum betrug 24 bzw. 72 Wochen.
Bei beiden Patienten nahm der entzündliche Rückenschmerz
und die periphere Gelenkbeteiligung deutlich ab. Die Beweglichkeit verbesserte
sich innerhalb eines halben Jahres um mehr als 50%, und auch die Laborwerte
verbesserten sich unter der Therapie.
Bei einem der Patienten verminderte sich nach 9 Monaten
Therapie die Zahl der weißen Blutkörperchen erheblich. Nach
Absätzen der Thalidomid-Therapie normalisierte sich die Leukozytenzahl
zügig, aber auch die Krankheitsaktivität stieg schnell wieder
an. Nach Wiederaufnahme der Therapie mit nur 100 mg Thalidomid pro
Tag ging die Krankheitsaktivität erneut zurück, ohne dass Nebenwirkungen
auftraten.
Studien zur Wirksamkeit von Thalidomid bei der
chronischen Polyarthritis wurden vor einigen Jahren eingestellt, weil die
Haupt(neben)wirkung von Thalidomid die Schlafneigung ist. Dies könnte
bei den vergleichsweise jüngeren Spondylitis-ankylosans-Patienten
aber anders sein.
Insgesamt könnte Thalidomid über die
indirekte Unterdrückung von TNF-alphaeinen
zweiten neuen Therapieansatz für die Spondylitis ankylosans darstellen.
Aber auch bei dieser Substanz sind zunächst kontrollierte Studien
zur Verträglichkeit und zum eindeutigen Wirksamkeitsnachweis notwendig.
Pamidronat gehört zur Gruppe der Aminobisphosphonate,
die dem Abbau der Knochensubstanz entgegenwirkt. Bisphosphonate
werden bei Erkrankungen mit verändertem Knochenstoffwechsel eingesetzt:
Beim Morbus Paget (einer Knochenkrankheit mit Verdickung
und Verkrümmung einzelner Röhrenknochen und Neigung zu Knochenbrüchen),
bei Knochenmetastasen und bei der Osteoporose.. Der Wirkungsmechanismus
ist bisher nicht eindeutig geklärt. Wesentlich ist eine Bindung an
die Oberfläche des Knochens mit Hemmung der Osteoklasten (für
den Knochenabbau zuständige Zellen). Neue Untersuchungen sprechen
dafür, dass Bisphosphonate auch entzündungshemmend wirken.
Im Tierversuch konnte durch Bisphosphonate eine Besserung hervorgerufen
werden.
1998 berichteten amerikanische Forscher erstmalig über
die Behandlung von 16 Spondylitis-ankylosans-Patienten mit Pamidronat.
Ihr Alter lag zwischen 27 und 62 Jahren (Durchschnitt 41,8 Jahre), die
durchschnittliche Erkrankungsdauer lag bei 12,3 Jahren (3 bis 32 Jahre).
Die Patienten hatten trotz der höchstzulässigen NSAR-Dosis eine
hohe Krankheitsaktivität (BASDAI durchschnittlich: 6,7). Drei Patienten
hatten gleichzeitig einen Morbus Crohn und erhielten eine Kombination aus
Paracetamol und Codein. Die 1. Gruppe mit 8 Patienten erhielt 30 mg Pamidronat
(Handelsname Aredia) monatlich über 3 Monate, gefolgt von Infusionen
mit 60 mg monatlich über weitere 3 Monate. Die 2. Gruppe mit ebenfalls
8 Patienten erhielt nur Infusionen mit 60 mg monatlich über 3 Monate.
Bezüglich der Krankheitsaktivität, der Wirbelsäulenbeweglichkeit
und der Blutsenkungsgeschwindigkeit wurden in der 1. Gruppe signifikante
Besserungen beobachtet. In der 2. (mit nur 3 Infusionen behandelten) Gruppe
war der therapeutische Effekt nicht sehr intensiv. Nur die Wirbelsäulenbeweglichkeit
hatte sich auch hier signifikant verbessert. Infusionsbegleitende Nebenwirkungen
waren Gelenkschmerzen und Fieber insbesondere bei der 1. Infusion. Sie
traten bei 50% der Patienten auf, waren aber leichtgradig und wurden außer
bei einem Patienten bei Folgeinfusionen nicht mehr beobachtet.
Diese ersten Ergebnisse sprechen dafür, dass Pamidronat
bei Spondylitis-ankylosans-Patienten insbesondere bei längerer Anwendung
eine entzündungshemmende Wirkung haben könnte. Damit ist auch
diese Substanz ein interessanter Kandidat für weitere Studien.
In den letzten 10 bis 20 Jahren konnte in einer Reihe großer Studien bei der rheumatoiden Arthritis (der chronischen Polyarthritis, einer ebenfalls entzündlich-rheumatischen Erkrankung) eindeutig belegt werden, dass Medikamente wie Methotrexat, Azathioprin und auch das neue Medikament Leflunomid eine anhaltende Unterdrückung der Entzündung und ein Aufhalten der Knochenzerstörung bewirken. Vergleichbar gute Untersuchungen liegen bei der Spondylitis ankylosans nicht vor. Es sollte zukünftig geklärt werden, ob nicht die eine oder andere dieser Substanzen auch für die Spondylitis ankylosans als Langzeit-Therapeutikum eingesetzt werden kann.
Die externe Strahlentherapie mit Röntgenstrahlen
ist bei der Spondylitis ankylosans in früheren Jahrzehnten durchaus
mit befriedigenden Ergebnissen zum Einsatz gekommen. Die Erfolgsquoten
lagen zwischen 40% bis 70%. Berichte über ein gegenüber der Normalbevölkerung
erhöhtes Leukämie-Risiko für die behandelten Patienten haben
ebenso wie die Entwicklung verträglicherer NSAR dazu geführt,
dass diese Behandlungsform bei der Spondylitis ankylosans deutlich zurückgegangen
ist und die Bestrahlung nur noch in Extremfällen erwogen wird.
Prinzipiell ist die externe Bestrahlung von der Injektions-Therapie
mit radioaktivem Radium-224 zu unterscheiden. Radium lagert sich
aufgrund der chemischen Ähnlichkeit zu Kalzium selektiv in Zonen vermehrten
Kalziumaustauschs ein. Infolge der geringen Reichweite der Alphastrahlung
wird fast nur das Zielgewebe bestrahlt (siehe Bechterew-Brief
Nr. 80 S. 1013). Dies ist ein ganz wesentlicher Vorteil gegenüber
der Röntgenbestrahlung, bei der stets das umliegende Gewebe mitbestrahlt
wird.
Die heute praktizierte Radium-224-Therapie mit Präparaten
hoher Reinheit in niedriger Dosierung von 280 Mikrocurie ist mit einem
deutlich geringeren Strahlenrisiko behaftet und stellt eine im Einzelfall
mögliche Behandlungsalternative dar. Allerdings sind auch hier prospektive
Studien notwendig, um den Stellenwert dieser Therapieform für die
Spondylitis ankylosans klarer festzulegen (siehe auch Bechterew-Brief
Nr. 81 S. 16 und Nr. 84 S. 32).
Anschrift der Verfasser: Klinikum Benjamin Franklin, Medizinische Klinik IV, Rheumatologie, Hindenburgdamm 30, 12200 Berlin
Quelle: Patientenverständliche Fassung eines in "Aktuelle Rheumatologie" Jahrgang 25 (2000) S. 38-42 erschienenen Aufsatzes
von Prof. Dr. med. Jürgen Braun, Dr. med. Jan Brandt und Prof. Dr. med. Jochen Sieper, Klinikum Benjamin Franklin der Freien Universität Berlin
Der Botenstoff TNF-alpha spielt für Entstehung und Aufrechterhaltung der Spondylitis ankylosans (Morbus Bechterew) nach heutigen Erkenntnissen eine wichtige Rolle. Seit einiger Zeit stehen jetzt Medikamente zur Verfügung, die TNF-alpha hemmen und teilweise unschädlich machen können. Eines davon heißt Infliximab. Es handelt sich um einen monoklonalen Antikörper, der durch molekulare Techniken hergestellt wird. Seine Wirksamkeit bei anderen chronisch entzündlichen Erkrankungen (chronische Polyarthritis, Morbus Crohn) wurde bereits nachgewiesen. In einer offenen Studie haben wir in Berlin deutliche Anhaltspunkte gewinnen können, dass Infliximab auch beim Morbus Bechterew wirksam ist. Ähnliche Ergebnisse liegen auch aus Belgien vor. Deshalb wird jetzt eine bundesweite Studie durchgeführt, an der folgende Zentren beteiligt sind:
Die Studie wird nach allen Regeln der Kunst doppelblind
und randomisiert durchgeführt. Das bedeutet, dass weder Arzt noch
Patient wissen, ob die Infusion, die zunächst nach 2 Wochen, nach
4 Wochen und dann alle 6 Wochen wiederholt wird, Infliximab enthält
oder nicht. In den ersten drei Monaten bekommt die Hälfte der Patienten
Placebo, also eine Infusion ohne den Wirkstoff. Dadurch kann man die kurzfristige
Wirksamkeit beweisen. Danach bekommt jeder Patient Infliximab für
ein Jahr. Damit können Erfahrungen in der Langzeitbehandlung gemacht
werden (bleibt die Wirksamkeit bestehen? reicht die Dosis? etc.).
Da Infliximab ein starkes gegen Entzündung
gerichtetes Medikament und kein Schmerzmittel ist, werden in die Studie
nur Patienten eingeschlossen, die sich in einer anhaltend aktiven Krankheitsphase
befinden. Wenn Sie sich in einem der Zentren vorstellen, wird dies anhand
bestimmter klinischer Zeichen am Anfang gemessen, um zu klären, ob
Sie für die Studie in Frage kommen. Studienbeginn ist im Juni 2000.
Eher nicht geeignet sind Patienten mit bereits sehr langer
Krankheitsdauer, schon ausgedehnten Verknöcherungen, wenig Schmerzen
und normalen Entzündungsparametern im Blut (C-reaktives Protein).
Wir hoffen, damit endlich ein wirksames Medikament gegen
den Morbus Bechterew gefunden zu haben.
Anschrift der Verfasser: Klinikum Benjamin Franklin, Medizinische Klinik IV, Rheumatologie, Hindenburgdamm 30, 12200 Berlin
von Prof. Dr. med. Jürgen Braun, Klinikum Benjamin Franklin der Freien Universität Berlin
Nicht-steroidale Antirheumatika (NSAR) wirken im wesentlichen durch
Hemmung des Enzyms Zyklooxygenase (COX), das bei der körpereigenen
Herstellung des Hor-mons Prostaglandin eine Rolle spielt. Sie wirken dadurch
entzündungshemmend, führen aber gleichzeitig zu einer verminderten
Widerstandsfähigkeit der Magenschleim-haut. Seit kurzem ist klar,
dass es zwei verschiedene Zyklooxygenasen gibt: COX-1 und COX-2. Zur Entzündungshemmung
und Schmerzlinderung ist es nötig, das Enzym COX-2 zu hemmen, während
COX-1 zum Schleimhautschutz beiträgt. Während ältere NSAR
wie Indometacin (Handelsname AMUNO) vor allem die COX-1 hemmen, beeinflussen
Diclofenac (VOLTAREN) und das etwas besser verträgliche Präparat
Meloxicam (MOBEC) vorzugsweise COX-2. Beide hemmen aber auch COX-1, vor
allem im höheren Dosis-Bereich. Das neuere NSAR Rofecoxib (Handelsname
VIOXX) ist dagegen ein spezifischer COX-2-Hemmer, der kaum noch eine nachweisbare
COX-1-Hemmung aufweist. Da aber auch dieses Präparat nur etwas weniger
auffällige Magen-Darm-Symptome erzeugt im Vergleich zu Diclofenac,
wird klar, dass die COX-1/COX-2-Unterscheidung nur ein Teil der Magen-Darm-Problematik
der NSAR erklärt.
Die selektive COX-2 Hemmung löst das Problem zwar nicht ganz.
Im Vergleich zu konventionellen Präparaten führt Rofecoxib, das
seit November 1999 für die Behandlung einer leichten Arthrose zugelassen
ist, aber zu einer deutlich geringeren Häufigkeit von Magengeschwüren.
Die Wirksamkeit der neuen COX-2-selektiven NSAR ist bei leichter Arthrose
dem Diclofenac oder Ibuprofen vergleichbar. Bei stärkeren Schmerz-
bzw. Entzündungszuständen ist sie wahrscheinlich eher als etwas
schwächer einzuschätzen. Für die Behandlung des Morbus Bechterew
liegen bezüglich der Wirksamkeit und Verträglichkeit bisher noch
keine Erkenntnisse vor.
Der Einsatz der neuen COX-2-selektiven NSAR wird aber auch durch ökonomische
Überlegungen relativiert, da die neuen Präparate, den erheblichen
Entwicklungskosten entsprechend, noch teurer sind als die konventionellen
Präparate. Ob die neueren COX-2-Hemmer sich bei ausgesprochenen Risikopatienten
(auch im Vergleich zu einer Kombination aus konventionellem NSAR und einem
Magenschutzmittel, z. B. Omeprazol) als günstiger erweisen, muss sich
in prospektiven Studien erst noch erweisen.